Структура атома
Что такое "атом"?
|
Атом - наименьшая частица элемента, обладающая его химическими свойствами |
До начала 20 века в науке бытовало мнение, что атом - неделимая частица. Однако, это оказалось не так. На самом деле в атом входят, так называемые, субатомные частицы. Для химиков особый интерес представляют: протон, нейтрон и электрон:
| Частица | Символ | Заряд | Масса (г) | Масса (а.е.м.) | Расположение |
| Протон | p+ | +1 | 1,673·10-24 | 1 | Ядро |
| Нейтрон | n0 | 0 | 1,675·10-24 | 1 | Ядро |
| Электрон | e- | -1 | 9,109·10-28 | 0,0005 | Вне ядра |
В основе атомной единицы массы (а.е.м.) лежит углеродная шкала-12. Атом углерода состоит из 6 протонов и 6 нейтронов и имеет атомную массу = 12 а.е.м. Отсюда, 1 а.е.м. = 1/12 части атома углерода.
Массы протонов и нейтронов практически равны. Масса электрона в 2000 раз меньше.
Несмотря на тот факт, что атом содержит как положительно заряженные частицы, так и отрицательно, его заряд нейтрален. Это объясняется тем, что в атоме одинаковое количество протонов и электронов. Разнозаряженные частицы нейтрализуют друг друга.
Ядро атома
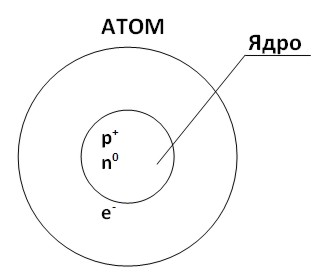
Эрнест Резерфорд в 1911 году предложил следующую модель атома: В центре находится положительно заряженное ядро, состоящее из протонов и нейтронов. Вокруг ядра вращаются электроны. Основная часть массы атома сосредоточена в ядре, которое имеет малый размер и чрезвычайно большую плотность (диаметр атома равен 10-10м; диаметр ядра атома = 10-15м). Говоря языком аллегорий: если представить атом в виде Олимпийского стадиона в Пекине, то ядро атома - это футбольный мяч, которым играют в футбол на этом стадионе.
Внимательный читатель задаст вопрос: "Если в ядре атома находятся положительно заряженные протоны, а одноименные заряды, как известно, отталкиваются, то почему ядро атома не разрушается?" Ученые пришли к выводу, что в ядре атома действуют некие, "склеивающие протоны", силы, которые и удерживают в целости ядро.
Т.к. ядро атома составляет основную массу атома, то массу атома можно считать равной сумме масс нейтронов и протонов.
|
Сумма протонов и нейтронов в ядре атома образует целое число - массовое число атома. Количество протонов атома - это порядковый (атомный) номер. |
Исходя из всего вышесказанного, глядя на структурный символ кислорода, можно смело сказать, что в его атоме присутствует 8 электронов.
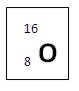
- O - химический символ элемента (кислород);
- 16 - массовое число;
- 8 - порядковый (атомный) номер.
Атомы одного элемента, имеющие один и тот же заряд ядра, но различные массовые числа, называются изотопами.
Изотопы водорода:
- 11H - протий;
- 12H - дейтерий;
- 13H - тритий;
Изотопы содержат одинаковое число протонов, но разное число нейтронов.
См. далее: Модель атома
