Свойства кислот и оснований
Распространенные кислоты:
- HCl - хлороводород (соляная кислота);
- H2SO4 - уксус;
- H2CO3 - серная кислота;
- CH3COOH - угольная кислота (газированная вода);
- H3BO3 - борная кислота (глазные капли);
- C16H12O6 - аспирин.
Распространенные основания:
- NH3 - нашатырный спирт (водный раствор аммиака);
- NaOH - гидроксид натрия (щелок);
- NaHCO3 - бикарбонат натрия (пищевая сода);
- CaCO3 - карбонат кальция.
Основные свойства кислот и оснований сведены в таблице:
| Кислоты | Основания | |
|---|---|---|
| На вкус | кислые | горькие |
| При попадании на кожу | вызывают ожог | вызывают ощущение намыленности |
| Вступают в реакцию | с металлами с образованием газообразного водорода | с маслами и жирами |
| Цвет индикатора | окрашивают лакмус в красный цвет | окрашивают лакмус в синий цвет |
| Образуют | диоксид углерода при соединении с пищевой содой | соль и воду при соединении с кислотами |
Приведенные выше свойства растворов кислот и оснований объясняют две основные теории: Аррениуса и Бренстеда-Лоури.
Теория Аррениуса
Сванте Аррениус разработал первую современную кислотно-основную теорию, которая, хоть и не лишена недостатков, но актуальна и по сей день.
Согласно теории Аррениуса:
- кислоты являются электролитами, которые диссоциируют с образованием ионов водорода, например: HCl→H++Cl-
- основания - это электролиты, которые диссоциируют в растворах с отщеплением гидроксид-ионов (ОН-), например: NaOH→Na++OH-
Поскольку, при смешивании водного раствора кислоты и основания получается нейтральный раствор, кислотно-основную реакцию Аррениус назвал реакцией нейтрализации.
HCl+NaOH → H2O+NaCl H++Cl-+Na++OH- → H2O+Na++Cl-
Ион водорода, взаимодействуя с гидроксид-ионом, образует молекулу воды (основной процесс, лежащий в основе кислотно-основных реакций Аррениуса):
H++OH- → H2O
Теория Аррениуса не лишена недостатков. Например, в результате взаимодействия газообразных аммиака с хлористым водородом образуется твердое вещество хлорид аммония:
NH3+HCl → NH4++Cl- → NH4Cl
В результате реакции соляная кислота передает аммиаку ион водорода, однако, данная реакция протекает в газовой фазе, а не в водном растворе (в ней не участвует гидроксид-ион), поэтому, ее нельзя отнести к кислотно-основным реакциям по Аррениусу.
Данную проблему решает протонная теория Бренстеда-Лоури, предложенная в 1923 году.
Теория Бренстеда-Лоури
Согласно теории Бренстеда-Лоури, кислота является донором, поставляя свои протоны водорода для образования химической связи, а основание выступает в роли акцептора, принимая эти протоны. Для образования донорно-акцепторной связи основание предоставляет одну пару своих электронов. Таким образом, ковалентная связь между кислотой и основанием образуется за счет двух электронов, которые изначально принадлежали одному атому, выступающего в качестве донора электронной пары, и свободной орбитали другого атома, выступающего в роли акцептора той же пары. Обычно ковалентная связь образуется из двух атомов, каждый из которых предоставляет по одному своему электрону, однако, при донорно-акцепторном способе формирования ковалентной связи оба электрона предоставляет один и тот же атом.
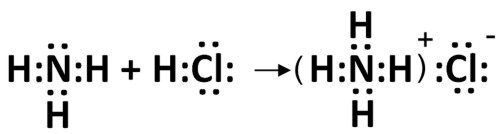
В ходе реакции взаимодействия NH3 и HCl, соляная кислота является донором протона, при этом аммиак и основание играют роль акцепторов, поскольку у аммиака имеется одна пара несвязанных электронов, которая используется для создания донорно-акцепторной связи.
Еще по теме:
