Атомы элементов 2(IIa) группы
| Элемент | Be | Mg | Ca | Sr | Ba | Ra |
|---|---|---|---|---|---|---|
| Порядковый номер | 4 | 12 | 20 | 38 | 56 | 88 |
| Атомная масса (относительная) | 9,01 | 24,30 | 40,08 | 87,62 | 137,33 | 226 |
| Плотность (н.у.), г/см3 | 1,85 | 1,74 | 1,55 | 2,54 | 3,5 | 5,5 |
| tпл, К | 1551 | 923 | 1112 | 1042 | 1022 | 1233 |
| tкип, К | 3243 | 1363 | 1757 | 1657 | 1910 | 2010 |
| Энергия ионизации, кДж/моль | 899,0 | 737,7 | 589,7 | 549,5 | 502,8 | 509,3 (1-й электрон) 979,0 (2-й) |
| Электронная формула | [He]2s2 | [Ne]3s2 | [Ar]4s2 | [Kr]5s2 | [Xe]6s2 | [Rn]7s2 |
| Электроотрицательность (по Поллингу) | 1,57 | 1,31 | 1,00 | 0,95 | 0,89 | 0,9 |
Электронные формулы инертных газов:
- He - 1s2;
- Ne - 1s22s22p6;
- Ar - 1s22s22p63s23p6;
- Kr - [Ar]3d104s24p6;
- Xe - [Kr]4d105s25p6;
- Rn - [Xe]4f145d106s26p6.
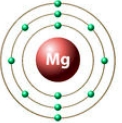
Рис. Строение атома магния.
Во 2 группу (IIa группу по старой классификации) периодической таблицы химических элементов Д. И. Менделеева входят 6 металлов: бериллий, магний, кальций, стронций, барий, радий (см. таблицу выше). Последние четыре - Ca, Sr, Ba, Ra называют щелочноземельными металлами, поскольку гидроксиды этих металлов обладают щелочными свойствами, а их оксиды по своей тугоплавкости похожи на оксиды тяжелых металлов, называемых ранее "землями".
Самым распространенным в земной коре элементом 2(IIa) группы является кальций (4,1% по массе), далее идут: магний (2,3%), барий (0,05%), стронций (0,037%), бериллий (0,00026%), радий (6·10-11).
Наиболее важным элементом подгруппы берилия является кальций, который входит в состав костей всех животных и человека, определяя их прочность. Концентрация ионов кальция и магния в воде определяет ее жесткость.
Элементы 2(IIa) группы в свободном виде в природе не встречаются, но входят в состав многих соединений:
- Be:
- 3BeO·Al2O3·SiO2 - минерал берилл;
- берилл с примесью Cr2O3 - изумруд;
- берилл с примесью Fe - аквамарин;
- (BeAl2)O4 - хризоберилл;
- (BeAl2)O4 с примесью Cr - александрит.
- Mg:
- MgCO3·CaCO3 - доломит;
- MgCO3 - магнезит;
- MgO·Al2O3 - шпинель;
- 2MgO·SiO3 - оливин;
- магний содержится в морской воде, а также входит в состав хлорофилла - важнейшей части фотосинтезирующего аппарата растений.
- Ca:
- CaCO3 - кальцит;
- CaSO4·2H2O - гипс;
- CaF2 - флюорит;
- Ca5(PO4)3F - фторапатит;
- Ca3(PO4)2 - фосфат кальция.
- Sr и Ba встречаются в виде карбонатов и сульфатов.
Физические свойства:
- металлы II группы имеют серебристо-белый цвет;
- низкую плотность (плотность увеличивается в подгруппе сверху-вниз);
- низкую температуру плавления (температуры плавления уменьшаются в подгруппе сверху-вниз);
- обладают высокой пластичностью;
- высокой электро- и теплопроводностью.
Все атомы элементов 2(IIa) группы на внешнем энергетическом уровне имеют по два валентных s-электрона (см. Электронная конфигурация атомов), с которыми в химических соединениях достаточно легко "расстаются", завершая, таким образом, свой внешний энергетический уровень, который становится устойчивым, по аналогии с завершенным энергетическим уровнем инертных газов.
Таким образом, отдавая "ненужные" валентные электроны (см. Валентность), элементы 2(IIa) группы в химических соединениях проявляют степень окисления +2, являясь сильными восстановителями, проявляя при этом высокую реакционную способность.
С ростом порядкового номера химического элемента увеличивается не только общее кол-во электронов (энергетических уровней), но также и радиус атома, что в свою очередь, обуславливает уменьшение энергии ионизации (соответственно усиление металлических свойств элемента) в направлении от бериллия к радию. В этом ряду активность металлов и их восстановительные свойства возрастают.
Наибольшее значение из всех шести элементов 2(IIa) группы имеют магний и кальций - металлы серебристо-белого цвета, мягкие и очень легкие, о них и пойдет речь дальше.
Химические свойства Mg, Ca
- при нагревании выше 600°C магний сгорает на воздухе ослепительно ярким белым пламенем (при н. у. магний защищен оксидной пленкой), с образованием оксида и нитрида магния:
O2 + 2Mg = 2MgO; N2 + 3Mg = Mg3N2; - кальций на влажном воздухе быстро реагирует с кислородом покрываясь рыхлой пленкой (смесь оксида и гидроксида кальция), при нагревании в кислороде воспламеняется:
O2 + 2Ca = 2CaO; - при н. у. легко реагируют с галогенами, образуя галогениды:
Ca + Cl2 = CaCl2; Mg + Cl2 = MgCl2; - при нагревании реагируют с неметаллами, образуя гидриды, нитриды, сульфиды, карбиды:
- H2 + Mg = MgH2;
- N2 + 3Ca = Ca3N2;
- S + Mg = MgS;
- 2C + Ca = CaC2.
- при кипячении магний вытесняет из воды водород, образуя гидроксид магния (кальций реагирует с водой при н. у.):
2H2O + Mg = Mg(OH)2 + H2; 2H2O + Ca = Ca(OH)2 + H2; - реагируют с соляной и разбавленной серной кислотой:
Ca + 2HCl = CaCl2 + H; Mg + H2SO4(рзб) = MgSO4 + H2; - реагируют с разбавленной азотной кислотой, образуя нитрат аммония:
4Mg + 10HNO3(рзб) = 4Mg(NO3)2 + NH4NO3 + 3H2O; - с концентрированной азотной кислотой (магний реагирует при нагревании):
4Mg + 10HNO3(кнц) = 4Mg(NO3)2 + N2O + 5H2O; - с концентрированной серной кислотой:
4Mg + 5H2SO4(кнц) = 4CaSO4 + H2S + 4H2O; - поскольку атомы элементов 2(IIa) группы являются сильными восстановителями, магний и кальций используются в реакциях восстановления металлов из их оксидов и галогенов, что находит широкое практическое применение в реакциях метллотермии, когда для получения редкоземельных металлов используют гораздо более распространенные щелочноземельные металлы:
- магнийтермия (в вакууме):
2RbCl + Ca = 2Rb + CaCl2; - кальцийтермия (в вакууме):
2CsCl + Mg = 2Cs + MgCl2.
- магнийтермия (в вакууме):
Оксиды и гидроксиды магния и кальция...
Получение магния и кальция
- электролизом расплавов солей: MgCl2 → Mg + Cl2;
- металлотермией (промышленный способ) при t>1200°C в электропечи в условиях вакуума, восстанавливая металлы из их соединений: 3CaO + 2Al = 3Ca + Al2O3;
- углетермией (восстановлением оксидов углем) в электропечи при t>2000°C: MgO + C = Mg + CO.
Применение
- Be:
- в качестве легирующей добавки к сплавам, придавая им твердость и прочность;
- как замедлитель и отражатель нейтронов в атомной промышленности.
- Mg:
- широко используется в конструкционных сверхлегких сплавах в автомобиле- и авиастроении;
- для получения редкоземельных металлов методом металлотермии;
- в органическом синтезе;
- в фото- и пиротехнике.
- Ca:
- в металлургии для удаления различных примесей при выплавке сталей и других сплавов;
- для получения редкоземельных металлов методом металлотермии;
- для выделения из воздуха инертных газов.
