Хлор (Cl)

- Обозначение - Cl (Chlorum);
- Период - III;
- Группа - 17 (VIIa);
- Атомная масса - 35,4527;
- Атомный номер - 17;
- Радиус атома = 99 пм;
- Ковалентный радиус = 102±4 пм;
- Распределение электронов - 1s22s22p63s23p5;
- t плавления = 100,95°C;
- t кипения = -34,55°C;
- Электроотрицательность (по Полингу/по Алпреду и Рохову) = 3,16/-;
- Степень окисления: +7, +6, +5, +4, +3, +1, 0, -1;
- Плотность (н. у.) = 3,21 г/см3;
- Молярный объем = 18,7 см3/моль.
- Уравнения окислительно-восстановительных реакций хлора (метод электронного баланса).
- Уравнения окислительно-восстановительных реакций хлора (метод полуреакций).
- Соляная кислота
Хлор в чистом виде впервые выделил шведский ученый Карл Шееле в 1774 году. Своё нынешнее название элемент получил в 1811 году, когда Г.Дэви предложил название "хлорин", которое вскоре было сокращено до "хлор" с легкой руки Ж. Гей-Люссака. Немецкий ученый Иоганн Швейгер предложил для хлора название "галоген", но этим термином было решено назвать всю группу элементов, в которую входит и хлор.
Хлор является самым распространенным галогеном в земной коре - на долю хлора приходится 0,025% всей массы атомов земной коры. По причине своей высокой активности хлор не встречается в природе в свободном виде, а только в составе соединений, при этом хлору "по барабану" с каким элементом вступать в реакцию, современной науке известны соединения хлора практически со всей таблицей Менделеева.
Основная масса хлора на Земле содержится в соленой воде Мирового океана (содержание 19 г/л). Из минералов больше всего хлора содержится в галите, сильвине, сильвините, бишофите, карналлите, каините.
Хлор играет важную роль в деятельности нервных клеток, а также в регуляции осмотических процессов, происходящих в организме человека и животных. Также хлор входит в состав зеленого вещества растений - хлорофилла.
Природный хлор состоит из смеси двух изотопов:
- 35Cl - 75,5%
- 37Cl - 24,5%
Хлор в Периодической таблице химических элементов Д. И. Менделеева, стоит под номером "17", относится к галогенам (См. Атомы элементов 17(VIIa) группы (галогены)).
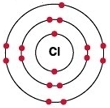
Рис. Строение атома хлора.
Электронная конфигурация атома хлора - 1s22s22p63s23p5 (см. Электронная структура атомов). В образовании химических связей с другими элементами могут участвовать 5 электронов, находящихся на внешнем 3p-уровне + 2 электрона 3s уровня (всего 7 электронов), поэтому в соединениях хлор может принимать степени окисления от +7 до -1. Как уже было сказано выше, хлор является химически активным галогеном.
Физические свойства хлора:
- при н.у. хлор является ядовитым газом желто-зеленого цвета с резким запахом;
- хлор в 2,5 раза тяжелее воздуха;
- при н.у. в 1 л воды растворяется 2,5 объема хлора - этот раствор называется хлорная вода.
Химические свойства хлора
Взаимодействие хлора с простыми веществами (Cl выступает в роли сильного окислителя):
- с водородом (реакция протекает только при наличии света):
Cl2+H2 = 2HCl
- с металлами с образованием хлоридов:
Cl20+2Na0 = 2Na+1Cl-1 3Cl20+2Fe0 = 2Fe+3Cl3-1
- с неметаллами, менее электроотрицательными, чем хлор:
Cl20+S0 = S+2Cl2-1 3Cl20+2P0 = 2P+3Cl3-1
- с азотом и кислородом хлор не реагирует непосредственно.
Взаимодействие хлора со сложными веществами:
Одной из самых известных реакций хлора со сложными веществами есть взаимодействие хлора с водой - кто живет в большом городе, наверняка, периодически сталкивается с ситуацией, когда, открыв кран с водой, ощущает стойкий запах хлора, после чего многие сетуют, дескать, опять воду хлорировали. Хлорирование воды является одним из основных способов ее обеззараживания от нежелательных микроорганизмов, небезопасных для здоровья человека. Почему так происходит? Разберем реакцию хлора с водой, которая протекает в два этапа:
- На первом этапе происходит образование двух кислот: соляной и хлорноватистой:
Cl20+H2O ↔ HCl-1+HCl+1O
- На втором этапе хлорноватистая кислота разлагается с выделением атомарного кислорода, который окисляет воду (убивая микроорганизмы) + подвергает отбеливающему действию ткани, окрашенные органическими красителями, если их опустить в хлорную воду:
HClO = HCl+[O] - реакция идет на свету
С кислотами хлор не взаимодействует.
Взаимодействие хлора с основаниями:
- на холоде:
Cl20+2NaOH = NaCl-1+NaCl+1O+H2O
- при нагревании:
3Cl20+6KOH = 5KCl-1+KCl+5O3+3H2O
- с бромидами металлов:
Cl3+2KBr = 2KCl+Br2↓
- с йодидами металлов:
Cl2+2KI = 2KCl+I2↓
- с фторидами металлов хлор не реагирует, по причине их более высокой окислительной способности, нежели у хлора.
Хлор "охотно" вступает в реакции с органическими веществами:
Cl2+CH4 → CH3Cl+HCl Cl2+C6H6 → C6H5Cl+HCl
В результате первой реакции с метаном, которая протекает на свету, образуется хлористый метил и соляная кислота. В результате второй реакции с бензолом, которая протекает в присутствии катализатора (AlCl3), образуется хлорбензол и соляная кислота.
- Уравнения окислительно-восстановительных реакций хлора (метод электронного баланса).
- Уравнения окислительно-восстановительных реакций хлора (метод полуреакций).
Получение и применение хлора
Промышленным способом хлор получают электролизом водного раствора (хлор выделяется на аноде; на катоде - водород) или расплава хлорида натрия (хлор выделяется на аноде; на катоде - натрий):
2NaCl+2H2O → Cl2↑+H2↑+2NaOH 2NaCl → Cl2↑+2Na
В лаборатории хлор получают действием концентрированной HCl на различные окислители при нагревании. В роли окислителей могут выступать оксид марганца, перманганат калия, бертолетова соль:
4HCl-1+Mn+4O2 = Mn+2Cl2+Cl20↑+2H2O 2KMn+7O4+16HCl-1 = 2KCl+2Mn+2Cl2+5Cl20↑+8H2O KCl+5O3+6HCl-1 = KCl+3Cl20↑+3H2O
Применение хлора:
- отбеливание тканей и бумаги;
- обеззараживание воды;
- производство пластмасс;
- производство хлорной извести, хлороформа, ядохимикатов, моющих средств, каучуков;
- синтез хлороводорода в производстве соляной кислоты.
См. далее: Соляная кислота
